第一条 为维护实验动物福利伦理,规范福利伦理审查工作,依据国家和地方有关实验动物福利伦理的法律、法规、标准等,根据中国食品药品检定研究院(简称中检院)实际工作情况,并参考国际惯例,制定本程序。
第二条 本程序适用于中检院涉及动物实验的检验工作和科研项目中的实验动物福利伦理申请和审查,以及实验动物生产繁育与使用的监督检查工作。
第三条 在中检院开展任何涉及实验动物的科研、教学及检验检测活动,均需在项目实施之前向实验动物福利伦理审查委员会(简称审查委员会)提出申请,接受审查。获得批准后方可进行有关工作,并接受监督检查。
第四条 审查委员会负责接受申请,依据实验动物福利伦理审查指导原则(简称指导原则)作出审查结论。
第五条 动物实验申请审查项目分为“一类项目”和“二类项目”两类。
一类项目:按照《中国药典》和有关技术规范而开展的检验项目等。
二类项目:包括涉及动物实验的科研项目(课题)、研究生课题以及为提高检验能力和检验水平而开展的各类研究工作。
第六条 申请
一类项目以科室为单位,由检验项目负责人按工作内容填写申请书(表格一)。
二类项目以课题或单项研究工作为单位,由项目负责人(或指定人员)填写申请书(表格二)。研究生开展的动物实验必须由其指导老师作为项目负责人。
提交申请书时,可提出对项目保密或审查公正性不利的委员回避。
第七条 受理
(一)审查委员会办公室接到申请书后,对申请书内容的完整性进行初审,即形式审查,在2个工作日内作出是否受理的答复。
(二)申请受理后生成审查编号。编号分为四个部分,格式为:
中检动(福)第年份编号(A为一类项目;B为二类项目)3位项目流水编号。
举例说明:中检动(福)第2017(A)001号,表示审查委员会2017年审查的第一个一类项目;中检动(福)第2017(B)001号,表示审查委员会2017年审查的第一个二类项目。
第八条 审查和签发
(一)一类项目:
初审后报主任委员或授权的副主任委员审核并签发审查结果。自申请书受理后3个工作日内完成审查和签发。项目审查情况由秘书汇总,在召开审查委员会会议时向大会汇报。
(二)二类项目:
由主任委员指派3名以上委员(至少包括相关领域的委员、兽医委员、公众代表委员),进行审查(表格三)。接到审查任务的委员应在5个工作日内给出审查意见。
项目负责人对审查委员会成员提出的改进要求须作积极回应(可以整改或者辩解),直到提出该整改要求的委员同意为止(表格四)。如果双方不能达成一致意见,项目负责人可将相关事项提交审查委员会讨论处理。审查委员会会议采取协商一致或少数服从多数的原则做出审查最终结论建议,不同审查意见将予以保留。必要时,审查委员会可要求申请者现场答疑。
由主任委员或授权的副主任委员签发审查结果。
(三)审查结果的签发以“实验动物福利伦理审查结果告知书”的形式书面通知申请人(表格五)。
如审查结果为“通过”,申请人可以按照申请书内容实施;如果审查结果为“未通过”,申请人可以选择放弃项目实施,或者根据审查意见,重新研究制定实验方案,再次提出申请。
第九条 变更
(一)一类项目:采取年度备案制,由项目负责人在项目批复到期日之前1个月内,对该项目依据、主要实验操作程序、实验人员等信息是否发生变更以及变更内容向审查委员会报备。
(二)已经获得审查批复同意开展的二类项目在实施中如内容或程序需要发生重大变动时,项目负责人应向审查委员会提交“变更申请”(表格六)。审查流程与首次申请一致。重大变动意外的情况,需要在变动发生后的一周内向审查委员会报备。
重大变更项目包括:
1. 项目负责人发生变更。
2. 涉及实验动物种类或数量的改变。
3. 涉及实验的关键操作流程发生改变。
4. 新增可能给动物或人员造成显著伤害的危险因素,包括试剂、操作、物理伤害等。
第十条 监督检查
对生产繁育、饲养和实验过程中实验动物福利伦理措施的落实情况进行定期或不定期的现场监督和检查,督促实验动物从业人员按照福利伦理审查指导原则的要求饲养和使用实验动物。
如发现存在有违反“指导原则”的行为,审查委员会将对项目负责人及具体的操作人员提出限期整改要求。在规定的期限内仍不改正者,经审查委员会集体讨论,可停止其参与实验动物生产或使用活动的资格。
如确因工作需要恢复其参与实验动物生产或使用活动资格的,由其本人所在科室负责人提出书面申请,经由审查委员会指定的培训机构培训考核合格后,恢复其参与实验动物生产或使用活动的资格。
第十一条 所有审查文件在项目结束后应归档保存。
第十二条 本程序由审查委员会负责解释
第十三条 本程序自公布之日起施行。
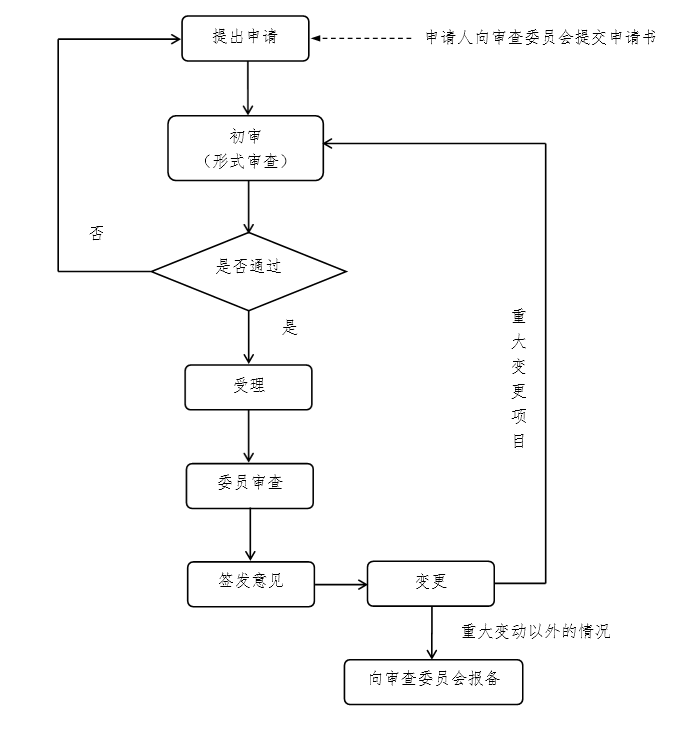
附件1:一类项目的审查流程
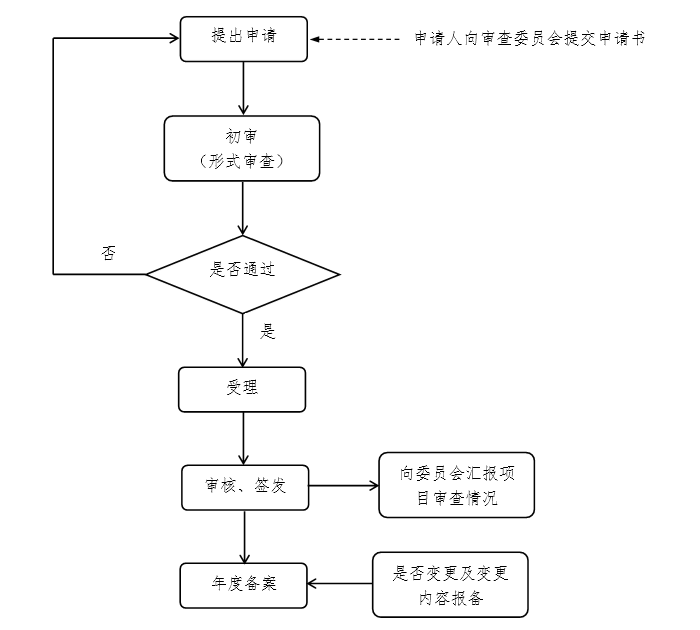
附件2:二类项目的审查流程